Objetivo
Aplicação dos conhecimentos de reações ácido-base na construção de um simples extintor de incêndio caseiro. Esse experimento pode ser realizado com o uso de materiais de fácil obtenção.
Materiais
a)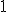 frasco de refrigerante de
frasco de refrigerante de  ;
;
b)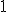 tubo de conta-gotas;
tubo de conta-gotas;
c)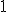 tubo de ensaio de
tubo de ensaio de  ;
;
d)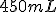 de vinagre;
de vinagre;
e) bicarbonato de sódio (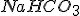 , pode ser comprado em qualquer seção de materiais de higiene bucal nos supermercados).
, pode ser comprado em qualquer seção de materiais de higiene bucal nos supermercados).
Procedimento
1. Com o auxílio de um estilete, fure a tampa do frasco de refrigerante de , no mesmo diâmetro do tubo de conta-gotas que será utilizado. A seguir, introduza o tubo de conta-gotas no orifício criado na tampa do frasco de refrigerante, como mostrado na figura 1.
, no mesmo diâmetro do tubo de conta-gotas que será utilizado. A seguir, introduza o tubo de conta-gotas no orifício criado na tampa do frasco de refrigerante, como mostrado na figura 1.
O furo feito na tampa deve permitir que o tubo de conta-gotas passe o mais justo possível, visando evitar vazamentos que podem prejudicar o experimento, devido à perda de reagentes (peça a ajuda de um adulto). O tubo de conta-gotas pode ser mais bem fixado com o uso de uma fita de teflon ao seu redor, antes de inseri-lo na tampa.
2. No frasco de refrigerante, coloque de vinagre comum e, no tubo de ensaio, adicione o bicarbonato de sódio de modo que o vinagre fique
de vinagre comum e, no tubo de ensaio, adicione o bicarbonato de sódio de modo que o vinagre fique 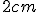 abaixo da borda do tubo (como mostra a figura 2).
abaixo da borda do tubo (como mostra a figura 2).
Tenha cuidado para que o bicarbonato de sódio não entre em contato com o vinagre, pois isso dará início imediato à reação química. Em seguida, feche o frasco de refrigerante com a tampa, mostrada na figura 1, apertando-a bem.
3. Para o extintor entrar em funcionamento, tampe o furo de saída do conta-gotas com o dedo indicador e sacuda vigorosamente o extintor, no intuito de provocar a reação química entre o vinagre e o bicarbonato de sódio.
4. Em seguida, incline o extintor para baixo, dirigindo-o para a região que você deseja atingir e tire o dedo da tampa, liberando assim a saída do líquido.
Entendendo o experimento
A construção do extintor de incêndio caseiro é uma aplicação das reações ácido-base em nosso cotidiano. O jato observado no extintor é o acetato de sódio ( ) juntamente com o ácido carbônico (que posteriormente se decompõe em gás carbônico e água) que são produzidos através da reação entre o ácido acético (
) juntamente com o ácido carbônico (que posteriormente se decompõe em gás carbônico e água) que são produzidos através da reação entre o ácido acético (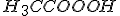 ) do presente no vinagre e o bicarbonato de sódio (NaHCO_3). Essa reação é representada pela seguinte equação química:
) do presente no vinagre e o bicarbonato de sódio (NaHCO_3). Essa reação é representada pela seguinte equação química:
+NaHCO_{3(s)}%20\rightarrow%20H_3CCOO^-Na^+_{(s)}+CO_2_{(g)}+H_2O) O gás produzido na reação (
O gás produzido na reação (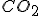 ) aumenta a pressão interna do extintor e, sendo esta maior do que a pressão externa, a água e o sal formados na reação são expelidos para fora do extintor.
) aumenta a pressão interna do extintor e, sendo esta maior do que a pressão externa, a água e o sal formados na reação são expelidos para fora do extintor.
Aplicação dos conhecimentos de reações ácido-base na construção de um simples extintor de incêndio caseiro. Esse experimento pode ser realizado com o uso de materiais de fácil obtenção.
a)
b)
c)
d)
e) bicarbonato de sódio (
1. Com o auxílio de um estilete, fure a tampa do frasco de refrigerante de
2. No frasco de refrigerante, coloque
3. Para o extintor entrar em funcionamento, tampe o furo de saída do conta-gotas com o dedo indicador e sacuda vigorosamente o extintor, no intuito de provocar a reação química entre o vinagre e o bicarbonato de sódio.
4. Em seguida, incline o extintor para baixo, dirigindo-o para a região que você deseja atingir e tire o dedo da tampa, liberando assim a saída do líquido.
Entendendo o experimento
A construção do extintor de incêndio caseiro é uma aplicação das reações ácido-base em nosso cotidiano. O jato observado no extintor é o acetato de sódio (
Comentários
Postar um comentário